Reneo Pharmaceuticals (RPHM)
Reneo Pharmaceuticals (RPHM)

Reneo Pharmaceuticals Inc. (RPHM)
Фармацевтическая компания специализируется на лечения пациентов с редкими генетическими митохондриальными заболеваниями.
Первоначально компания разрабатывает REN001 для лечения трех редких генетических заболеваний, которые обычно проявляются миопатией и связаны с высокими неудовлетворенными медицинскими потребностями: первичные митохондриальные миопатии (PMM), нарушения окисления длинноцепочечных жирных кислот (LC-FAOD) и болезнь накопления гликогена V типа (McArdle болезнь).
Деятельность: фармацевтика
Сотрудники: 23
Год основания: 2014 г.
Контактная информация
Адрес: 12230 El Camino Real, Suite 230 Сан-Диего, Калифорния 92130
Телефон: (858) 283-0280
Веб-сайт: www.reneopharma.com
Финансовая информация
Рыночная капитализация: 387,36 млн. $
Выручка: $ 0 млн. (за последние 12 месяцев)
Чистая прибыль: -19,5 млн. долларов США (за последние 12 месяцев)
Профиль IPO
Акции (в миллионах): 6,3
Ценовой диапазон: $ 15,00 - $ 17,00
Объем: $ 100,0 млн.
Менеджер/Совместные менеджеры: Jefferies/ SVB Leerink/ Piper Sandler
СО-менеджеры: -
Тикер: RPHM
Биржа: NASDAQ
Дата выхода: 09.04.2021

О Компании Reneo Pharmaceuticals Inc. (RPHM)
Компания разрабатывает генетические методы лечения пациентов, страдающих митохондриальными заболеваниями.
Согласно заявлению о регистрации S-1, Reneo Pharmaceuticals (RPHM) подала заявку на привлечение 100 миллионов долларов в ходе IPO своих обыкновенных акций.
Компания и технологии
Компания Reneo из Сан-Диего, штат Калифорния, была основана для разработки методов генетической модуляции генов, ответственных за метаболизм и выработку АТФ (аденозинтрифосфата), который используется в качестве источника энергии для клеточных процессов.
Компания завершила клиническое испытание фазы 1b с участием пациентов с PMM, и предварительные результаты показали, что лечение REN001 хорошо переносится, улучшает физическую работоспособность, увеличивает потребление кислорода и выносливость, а также улучшает симптомы, о которых сообщают пациенты. Компания начала глобальное клиническое исследование фазы 2b у пациентов с PMM и планируем начать набор в первой половине 2021 года. Также Reneo планируем провести долгосрочное исследование безопасности на подгруппе пациентов из клинического исследования фазы 2b. Компания ожидает результаты этих клинических испытаний в 2023 году. Основываясь на взаимодействии с США и несколькими европейскими регулирующими органами, и полагает, что положительные результаты этих испытаний могут поддержать регистрацию REN001 для PMM как в Соединенных Штатах, так и в Европе.
Также компания проводит два клинических испытания фазы 1b REN001 у пациентов с LC-FAOD и болезнью Макардла соответственно. Оба клинических испытания фазы 1b в настоящее время регистрируются, и они ожидают результаты в первой половине 2022 года. Компания также планируем изучить потенциал REN001 при других редких заболеваниях, таких как мышечная дистрофия Дюшенна и синдром Альпорта, по которым у нихесть подтверждающие доклинические данные.
В следующей таблице приведены сведения о конвейере для REN001: 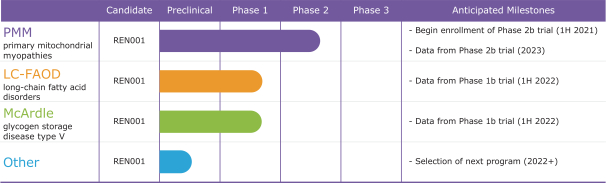
REN001 Обзор
REN001 разработан для избирательной активации рецепторов PPARd, обнаруженных в ядерной мембране мышечных и других клеток. PPARd является членом семейства ядерных рецепторов, которые регулируют выработку клеточной энергии, модулируя экспрессию генов, контролирующих белки, участвующие в активности митохондриальных ферментов и образование новых митохондрий (митохондриальный биогенез). PPARd высоко экспрессируется в мышечных клетках, и было показано, что активация PPARd либо посредством генетических манипуляций, либо с помощью низкомолекулярных агонистов увеличивает способность мышечных клеток использовать жирные кислоты, а также улучшает мышечную силу и толерантность к физической нагрузке у исследуемых животных. Reneo считает, что механизмы с помощью которых REN001 будет действовать, будет способен помочь пациентам с митохондриальными заболеваниями.
Первоначально компания разрабатывает REN001 при следующих трех редких генетических заболеваниях, которые связаны с дефицитом выработки энергии в митохондриях и обычно проявляются миопатией:
1) PMM: это редкое заболевание, по оценкам, распространенность около 100 000 пациентов в Соединенных Штатах и Европе вместе взятых. Пациенты с PMM не могут эффективно двигать мышцами, потому что их способность генерировать энергию посредством окислительного фосфорилирования (OxPhos) нарушена. Reneo нацелена на лечение взрослых пациентов с PMM, у которых есть дефекты митохондриальных генов, связанные с миопатией, недостаточной выносливостью, непереносимостью физических упражнений и утомляемостью.
2)LC-FAOD: это редкое заболевание, по оценкам, распространенность которого составляет около 15 000 пациентов в Соединенных Штатах и Европе вместе взятых. Генетические изменения, наблюдаемые у этих пациентов, снижают их способность метаболизировать длинноцепочечные жирные кислоты как источник энергии для митохондрий. По мере того как пациенты с LC-FAOD становятся старше, они страдают миопатией, недостаточной выносливостью, непереносимостью физических упражнений и утомляемостью. Напряжение мышц при отсутствии адекватного источника энергии может привести к разрушению мышечной ткани, что впоследствии может вызвать повреждение почек и сердца.
3) Болезнь Макардла: это редкое заболевание, по оценкам, его распространенность составляет около 11 000 пациентов в Соединенных Штатах и Европе вместе взятых. Пациенты с болезнью Макардла имеют особую неспособность расщеплять гликоген до глюкозы как источника энергии для митохондрий. Пациенты с болезнью Макардла испытывают мышечные повреждения с сильной острой усталостью и мышечной болью. Разрушение мышечной ткани также может вызвать повреждение почек.
Мышечные клетки в основном полагаются на три источника энергии: фосфокреатин, углеводы (гликоген) и жирные кислоты. В начале нагрузки мышечные клетки используют легкодоступные источники энергии, такие как фосфокреатин и углеводы (гликоген). По мере того, как эти источники энергии истощаются при постоянном напряжении, мышечные клетки превращаются в жирные кислоты в качестве основного источника для выработки энергии.
Митохондрии отвечают за выработку большей части энергии для клеток в форме АТФ. Клетки имеют от сотен до тысяч митохондрий, причем каждая митохондрия содержит белки, полученные как из ядерных, так и из митохондриальных генов. Пациенты с PMM могут иметь дефекты ядерных или митохондриальных генов, которые приводят к снижению производства энергии в митохондриях. Пациенты с LC-FAOD имеют дефицит ферментов, расщепляющих длинноцепочечные жирные кислоты, что приводит к дефициту энергии. Пациенты с обоими этими заболеваниями страдают от недостатка выносливости, утомляемости и мышечной слабости, и они не могут эффективно двигать мышцами, потому что их способность генерировать энергию с помощью OxPhos находится под угрозой. Терапия очень ограничена для пациентов с редкими генетическими митохондриальными заболеваниями и состоит в основном из диеты и пищевых добавок для обеспечения альтернативных источников энергии, а также тщательно контролируемого режима упражнений. Повышение способности этих пациентов метаболизировать жирные кислоты потенциально может снизить их энергетический дефицит и улучшить их способность функционировать.
Пациенты с болезнью Макардла не могут расщеплять гликоген в мышцах. Пациенты с болезнью Макардла жалуются на сильную острую боль и трудности с движением мышц после первых нескольких минут мышечной активности. Увеличение метаболизма жирных кислот может позволить пациентам преодолеть дефицит гликогена, тем самым минимизируя недостаток энергии, связанный с их заболеванием.
Руководство возглавляет президент и генеральный директор Грегори Флешер, который работает в компании с 2020 года и ранее был генеральным директором Novus Therapeutics и Otic Pharma.
Источник: Mitocon Odv
Фирма продвигает REN001 через испытания различных программ для лечения пациентов с первичными митохондриальными миопатиями и другими родственными состояниями.
REN001 готовится к участию в испытаниях фазы 2b, основанных на успешной безопасности и первоначальной эффективности его усилий на фазе 1, которые показали увеличение расстояния ходьбы пациента, потребление кислорода и снижение утомляемости и боли.
Ниже представлен текущий статус разработки лекарств компании: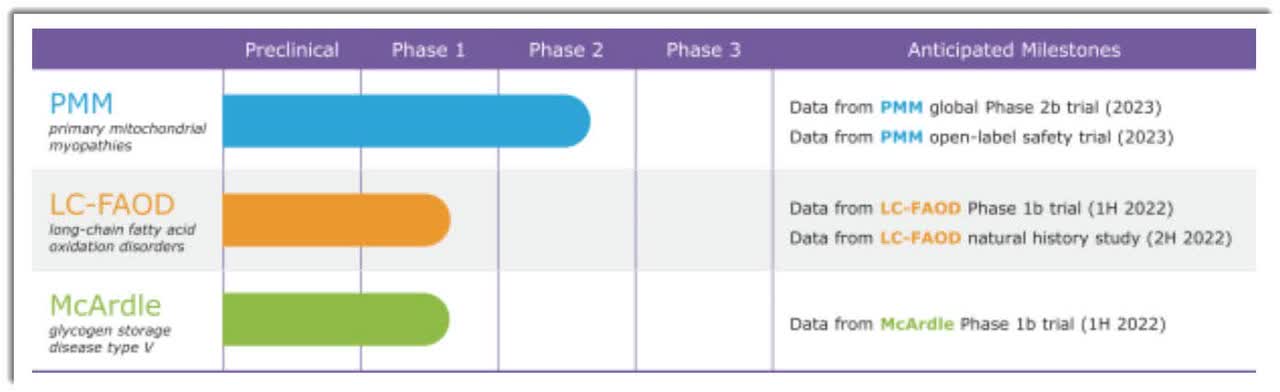
Источник: данные компании SEC Filing.
Инвесторы в фирму вложили не менее 93 миллионов долларов и включают New Enterprise Associates, Novo Holdings, RiverVest, Lundbeckfond Invest A / S и Abingworth Bioventures.
Рынок и конкуренция
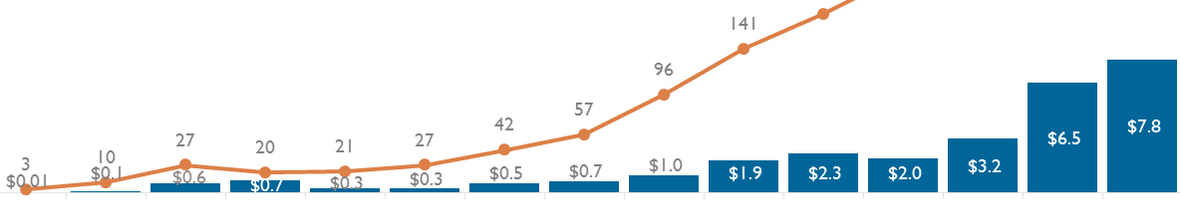
Согласно отчету Market Research Future об исследовании рынка за 2021 год, к 2023 году мировой рынок средств лечения митохондриальной миопатии достигнет 600 миллионов долларов.
Это представляет собой прогноз CAGR (совокупный годовой темп роста) в 3,2% с 2017 по 2023 год.
Ключевыми элементами, способствующими этому ожидаемому росту, являются увеличение числа выявленных случаев за счет улучшения возможностей скрининга, а также улучшение лечения за счет государственных стимулов, направленных на продвижение разработки лечения редких генетических заболеваний.
Кроме того, на долю США приходится самая высокая доля рынка благодаря благоприятным компенсациям, в то время как Европа занимает второе место по спросу. Ожидается, что в Азиатско-Тихоокеанском регионе спрос будет расти самыми быстрыми темпами до 2023 года.
Основные конкурирующие поставщики, которые предоставляют или разрабатывают соответствующие методы лечения, включают:
Reata Pharmaceuticals (NASDAQ:RETA)
Stealth BioTherapeutics (NASDAQ:MITO)
Raptor Pharmaceutical Corp.
GeneDx
NeuroVive Pharmaceutical
Abliva AB (OTCPK:NEVPF)
Cyclerion Therapeutics (NASDAQ:CYCN)
Khondrion B.V.
Финансовые показатели
Недавние финансовые результаты Reneo типичны для биофармацевтической фирмы, работающей на клинической стадии, поскольку они не показывают доходов и значительных затрат на НИОКР и G&A, связанных с ее усилиями по разработке трубопроводов.
Ниже приведены финансовые результаты компании за последние два года: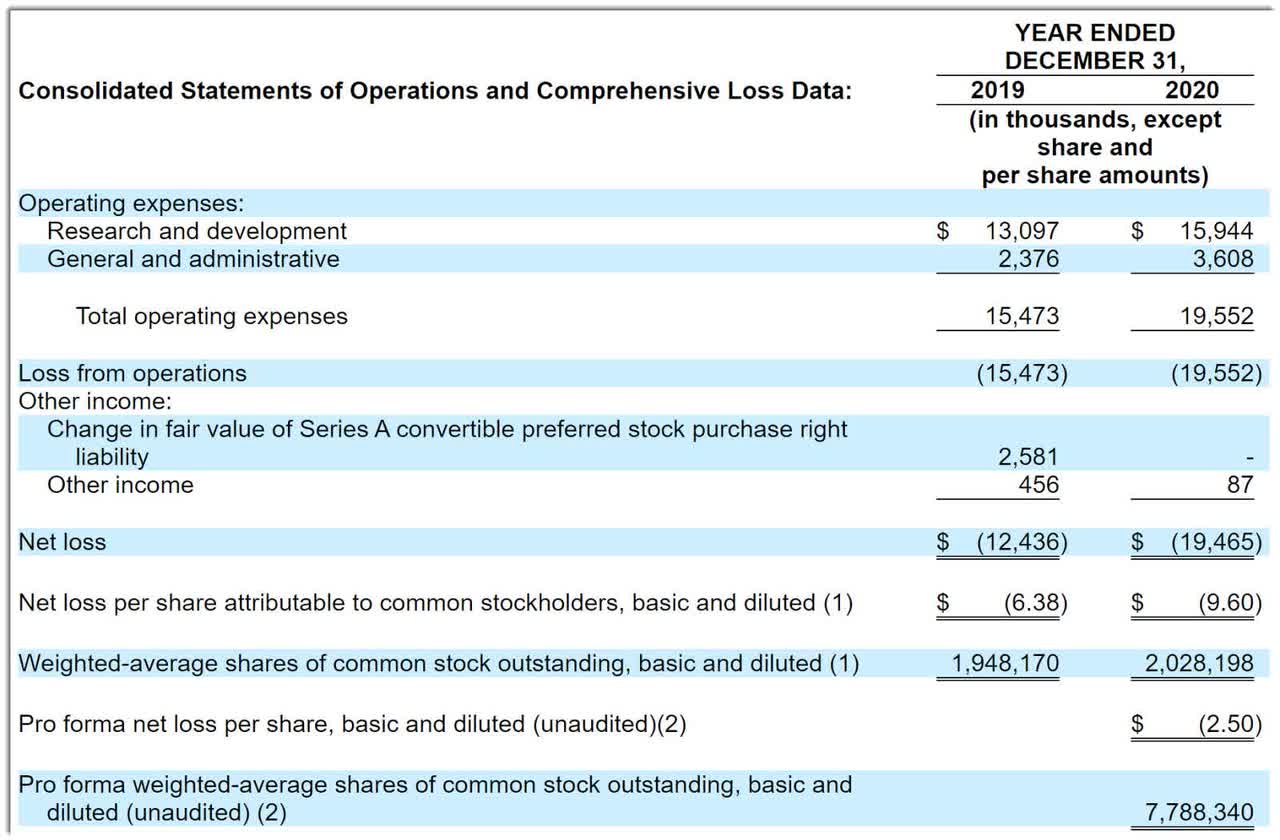
Источник: Заявление о регистрации компании.
По состоянию на 31 декабря 2020 года у компании было 53,6 млн долларов наличными и 4,6 млн долларов в совокупных обязательствах.
Детали IPO
Reneo намеревается привлечь 100 миллионов долларов валовой выручки от IPO своих обыкновенных акций, предложив 6,25 миллиона акций по средней предложенной цене в 16,00 долларов за акцию.
В случае успешного IPO стоимость компании при IPO составит около 333,8 миллиона долларов, без учета опционов андеррайтера на избыточное размещение.
Без учета опционов андеррайтеров и частных размещаемых акций или акций с ограниченным доступом, если таковые имеются, отношение количества размещенных к обращению акций составит примерно 25,82%.
Руководство заявляет, что оно будет использовать чистую выручку от IPO следующим образом:
1) около 20,0 миллионов долларов США на финансирование исследований и разработок REN001 в PMM, включая завершение нашего глобального клинического исследования фазы 2b REN001 на пациентах с PMM и нашего запланированного долгосрочного исследования безопасности REN001 за пределами США у пациентов из клинической фазы 2b пробный;
2) приблизительно 15,0 миллионов долларов на финансирование исследований и разработок REN001 у пациентов с LC-FAOD, включая завершение нашего клинического исследования фазы 1b;
3) приблизительно 15,0 миллионов долларов для финансирования исследований и разработки REN001 у пациентов с болезнью Макардла, включая завершение нашего клинического испытания фазы 1b; и
4) оставшаяся выручка направлена на подготовку к коммерческой готовности, на другие научно-исследовательские и опытно-конструкторские работы, на оборотный капитал и на общие корпоративные цели.

Список предыдущих IPO 2021: